自然界中众多重要的生物成分呈现出介观螺旋结构,包括由D-糖构成的P-双螺旋DNA,以及由L-氨基酸构建的P-α-螺旋和三链M-螺旋胶原蛋白等。然而,尽管这些螺旋结构对生命过程至关重要,但复杂的结构使得人们对小分子如何决定这些螺旋结构的手性因素了解甚少。手性分子诱导向列相液晶(LCs)形成螺旋超结构,为模拟这些系统中手性转移复杂性提供了良好模型。对于胆甾相结构而言,具有圆偏振发光(CPL)活性的液晶由于其卓越的发光不对称因子带来的潜在应用而备受关注。其中,二元手性液晶因其手性发光体同时具有手性和发光的性能,可以有效避免过度掺杂导致胆甾相结构受到破坏。近年来,科研人员开发了许多手性发光材料作为手性诱导剂的二元手性液晶材料。然而,这些材料的掺杂剂都不能够调节光子禁带的位置来匹配其发射,导致其较低的发光不对称因子(glum)。因此,开发具有高螺旋扭曲力的手性发光诱导剂仍然是设计圆偏振发光材料中至关重要的问题。
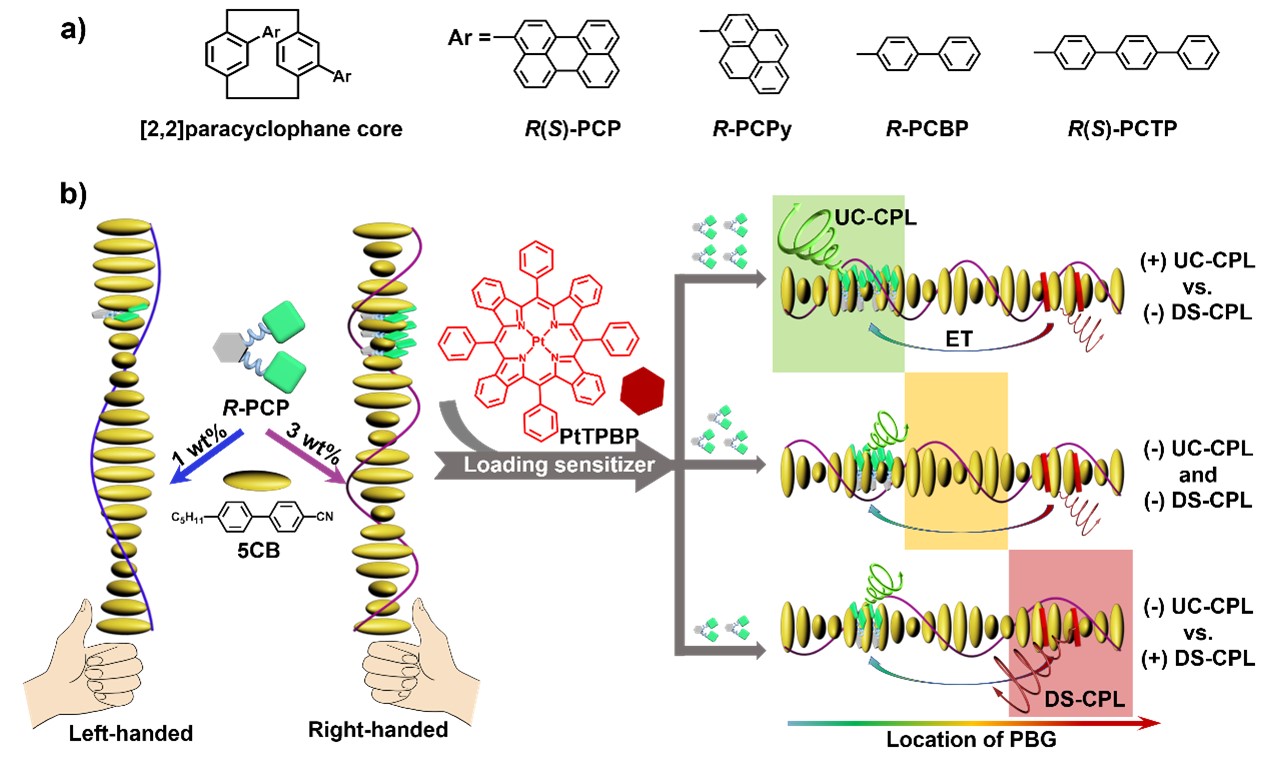
图一: (a)各种对环芳烃类平面手性发射体的化学结构。(b)向列相液晶(5CB)中掺杂不同量的手性荧光分子(R-PCP)可导致螺旋方向反转。此外,引入敏化剂- PtTPBP将同时实现基于R-PCP的三重-三重湮灭的CPL上转换(UC-CPL)和PtTPBP的下转换CPL (DS-CPL)。液晶中不同浓度的R-PCP导致光子带隙(PBG)位置可调,从而产生UC-CPL和DS-CPL,与液晶本身呈现相反的圆偏振方向。彩色背景代表了不同波长范围的PBG。ET:从PtTPBP到R-PCP的三重态-三重态能量转移。
国家纳米科学中心段鹏飞课题组通过控制一系列基于对环芳烃的手性发射体在液晶中的掺杂量来实现CPL的反转和放大(如图一所示)。结果表明,单一手性发射体可以通过分子尺度上的浓度依赖效应在宏观水平上诱导胆甾相螺旋方向反转。具体来说,这些手性分子在低掺杂比例时优先与LC分子形成相反手性的高阶胆甾相结构。在高掺杂比例下,手性诱导剂以一定的旋转优先嵌入对方,形成了一种新的手性物种。当分子满足描述的一些参数时,新的手性物种表现出与单体状态相反的手性,且与液晶分子相互作用时形成与单体相反的胆甾相结构。(如图二所示)
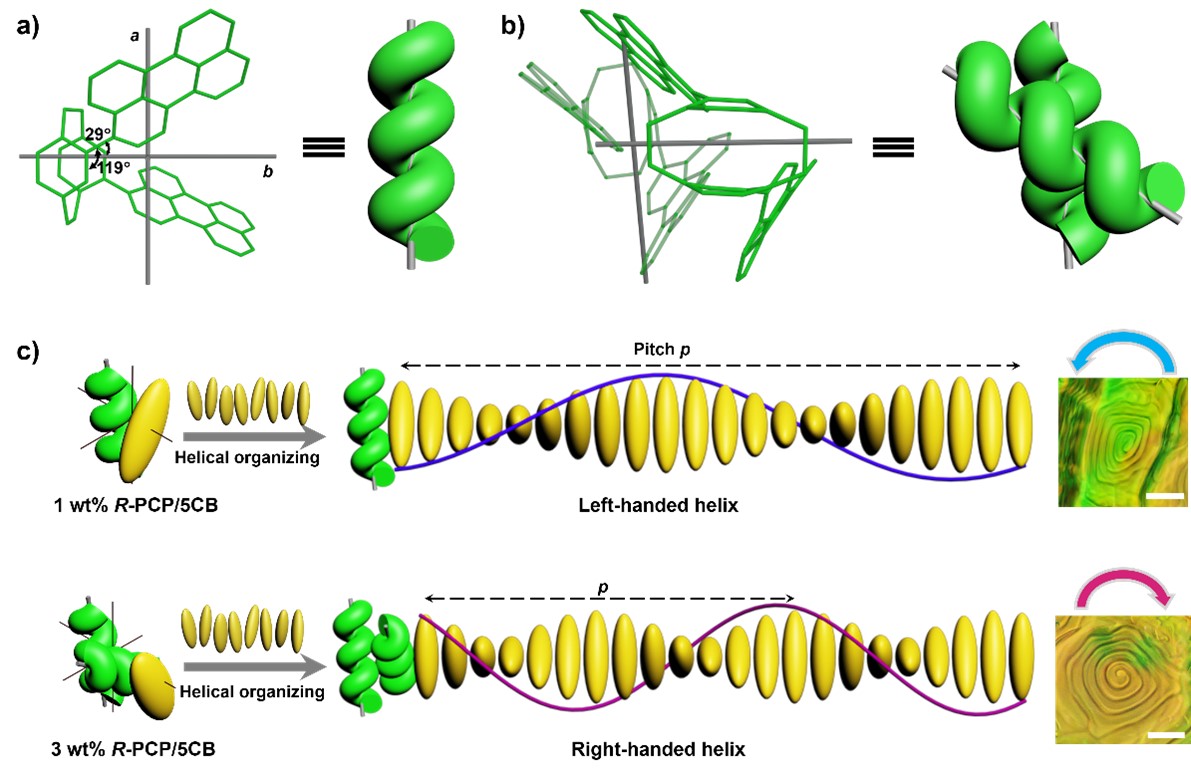
图二:(a) R-PCP的双轴分子结构(省略氢原子)及其基于Emelyanenko方法模拟出分子轴为a的右手螺旋模型。(b) R-PCP二聚体(省略氢原子)及其分子模型的优化模拟。(c) 1 wt% R-PCP/5CB和3 wt% R-PCP/5CB的手性诱导和介观组装示意图。
此外,由于这些分子具有高的HTP,能够调节胆甾相的光子禁带至短波长区域,甚至能够与其发光峰匹配,从而产生的CPL具有极高的发光不对称因子(glum = 1.2)。基于这一特性设计了一个三元手性LCs体系,通过调节R-PCP的相互浓度,在同一个胆甾相中实现了兼具上转换圆偏振发光(UC-CPL)和下转移圆偏振发光(DS-CPL)的双重圆偏振发射。尽管控制微观手性相互作用到宏观手性信息传递的潜在机制仍有待进一步研究,但这一创新系统模型为人们理解这种分子手性到结构手性的传递提供了全新的见解,而推动新一代手性材料和先进光子器件的开发和制造。(文章链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202315136)
转载文章请注明出处:国家纳米科学中心段鹏飞老师课题组 https://duanpengfei-chirality.com/